摘 要 近年来,双氧水在食品加工过程中被广泛使用,但如果食品中残留过量双氧水对人体则有较大危害。更值得关注的是,一些生产企业违规向食品中添加工业级双氧水用于漂白和杀菌。工业双氧水含有危及食品安全的有害物质,如2-乙基蒽醌和过量的重金属等。我国现有相关标准中,至今尚无关于食品中残留双氧水的检测方法。已有的工业废水中2-乙基蒽醌的检测和药物中蒽醌的检测方法,对于食品中微量2-乙基蒽醌的检测不太适用。笔者在工作实践中发现,食品中残留双氧水的检测,可以采用扣除背景的高锰酸钾氧化法,食品中2-乙基蒽醌的检测可采用有机溶剂萃取的高效液相色谱法。
关键词 食品 双氧水 2-乙基蒽醌 检测
研究的目的
双氧水(学名过氧化氢)属于强烈的氧化剂,作为生产加工助剂,具有消毒、杀菌、漂白等功能。
双氧水有食品级双氧水和工业级双氧水之分。食品级双氧水为电解法制造,具有纯度高、杂质少、稳定性好、无有毒有害杂质。但加入过量的双氧水(无论是哪个级别的)都将导致食品营养成分损失,同时较大量的双氧水残留对人体也极为不利。食品中双氧水的检测是确保食品安全所需要的。工业级双氧水主要采用2-乙基蒽醌+钯催化生产,其中含有大量2-乙基蒽醌以及铅、砷等金属离子、机械杂质等。这些有毒有害杂质中,2-乙基蒽醌、铅、砷是致癌物质,因此,工业级双氧水不能用于食品行业。
近年来,食品级双氧水在食品加工过程中被广泛使用。如用双氧水对鱼翅、开心果等进行漂白,对牛奶和奶制品杀菌,对饮用水进行灭菌消毒等。由于食品级双氧水的生产具有一定的技术难度,价格比工业级双氧水高得多,一些企业在食品的生产加工过程中违规使用工业级双氧水。
我国现有相关标准中,至今尚无关于食品中双氧水、2-乙基蒽醌的检验方法。GB2760《食品添加剂使用卫生标准》及其系列修订版本也没有给出普通食品中残留双氧水的规范限定。尽管纯净双氧水、药品中高含量蒽醌已经有了检测方法。但是,食品中有许多成分(如钙离子、维生素、还原糖甚至不饱和脂肪酸等)对食品中双氧水的检测结果有不可忽略的影响。工业废水和药品中的高含量蒽醌的检测方法对食品中微量的2-乙基蒽醌残留量的检测不太适用。因此,食品中的双氧水、2-乙基蒽醌残留量的检测方法不能完全照搬现有非食品的方法,所以研究出提纯或防止干扰的检测方法很有必要。
研究结果
1 食品中双氧水残留量的检测
1.1主要试剂
高锰酸钾标准溶液:使用分析纯高锰酸钾配制成0.1mol/L标准溶液,用草酸钠标准溶液标定。
草酸钠标准溶液:使用基准草酸钠配制成0.1mol/L标准溶液。
草酸标准溶液:使用基准草酸配制成0.1mol/L标准溶液。
过氧化氢标准溶液:吸取35ml30%过氧化氢(分析纯)溶液用蒸馏水稀释至1l。用草酸标准溶液标定。
1.2主要仪器
电子分析天平、真空泵、离心机(3000转/分)、酸式滴定管、电炉
1.3方法原理
取3份样品,第1份不经加热处理,第2份加热除去双氧水,第3份加热蒸馏取馏出液测定,前两份样品消耗高锰酸钾标准溶液(或草酸标准溶液)量的差再减去第3份试样所消耗的高锰酸钾标准溶液的体积,计算出双氧水的含量。
化学方程式:H2O2+KMnO4+4H+=MnO2+2KOH+2H2O
1.4 分析步骤
1.4.1样品处理
1.4.1.1对于澄清透明的液态样品,分别吸取样品25ml样品用于检测。
1.4.1.2对于非澄清的液态样品,吸50ml样品于100ml容量瓶中,加10.6%亚铁氰化钾溶液和20%乙酸锌溶液各4ml,摇匀,静置,过滤。吸取25ml滤液用于检测。
1.4.1.3对于脂肪含量高的样品,称取2~5克样品,于烧杯中加水搅拌萃取,然后用滤纸过滤,并用水反复冲洗滤纸上的残留物,收集水相定容至100ml,吸取25 ml (或50ml)用于检测。
1.4.2测定
将第1份样品预处理后,在室温下加50ml水和10ml1+1硫酸溶液,用0.2mol/L的高锰酸钾标准溶液滴定至微红色出现,30秒不退色为止。
第2份样品预处理后,加热煮沸10分钟,冷却后从上一步的“加50ml水”开始操作。
第3份样品处理后的试液置于全玻璃蒸馏装置中,加150ml水,加热蒸馏,收集约100ml馏出液,从第1份样品中操作方法的“10ml1+1硫酸溶液”开始操作。
1.4.3 计算公式
食品中双氧水含量
(V1-V2-V3)×c×34.0
V0
式中:V0——检测时所吸取的原始样品的体积(ml);
V1——滴定冷试液所消耗的高锰酸钾标准溶液的体积(ml);
V2——滴定加热煮沸后的试液所消耗的高锰酸钾标准溶液的体积(ml);
V3——滴定收集的挥发酸馏出液所消耗的高锰酸钾标准溶液的体积(ml);
c——高锰酸钾标准溶液的浓度(mol/L);
34.0——1摩尔过氧化氢的质量(g/mol)。
1.5 回收率试验
以清水板栗罐头的汤汁为背景,做加标回收率试验,结果如表1所示。
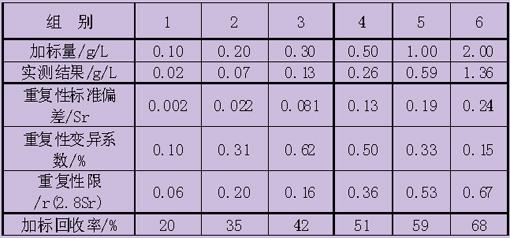
表1 食品中双氧水检测的加标回收率试验结果
2 食品中2-乙基蒽醌的检测
2.1主要试剂
甲醇(色谱纯);氯仿(分析纯);丙酮(分析纯);乙醚(分析纯);石油醚(分析纯,60~90℃));亚铁氰化钾沉淀剂:用蒸馏水溶解亚铁氰化钾(分析纯)配成10.6%的水溶液,贮存于综色试剂瓶中;乙酸锌20%水溶液:用蒸馏水溶解乙酸锌(分析纯)配成20%的水溶液;2-乙基蒽醌标准溶液:用2-乙基蒽醌对照品配成。
2.2主要仪器
电子分析天平、高效液相色谱仪(带紫外检测器,C-18反相色谱柱)、真空泵、离心机(3000转/分)
2.3方法原理
样品经处理后,用有机溶剂萃取。进高效液相色谱仪,利用保留时间定性,峰面积定量。
2.4分析步骤
2.4.1样品处理
2.4.1.1对于澄清透明的液态样品,吸取样品5ml,用三氯甲烷萃取3次,每次5ml,剧烈振摇1min。合并收集的三氯甲烷,放于刻度试管中,水浴挥干,加2~5ml三氯甲烷超声波溶解。
2.4.1.2对于固态样品,准确称取2.0克样品,加15ml三氯甲烷(或丙酮),盖紧瓶塞,振荡30min。以下操作同2.4.1.1“放于刻度试管中”之后的操作。
2.4.1.3对于非澄清的液态样品,吸取50ml样品于100ml容量瓶中,加10.6%亚铁氰化钾溶液和20%乙酸锌溶液各4ml,摇匀,静置,过滤。吸取10ml滤液,按2.4.1.1操作。
2.4.1.4对于脂肪含量高的样品,称取2~5克样品,于烧杯中加甲醇搅拌,过滤,用甲醇反复冲洗滤纸,收集甲醇滤液减压浓缩至合适的体积。然后视试液的澄清情况,按2.4.1.1或2.4.1.3处理。
2.4.2高效液相色谱条件
柱:反相C-18
流动相:甲醇
流速:1ml/min
检测器:紫外检测器,波长254nm
2.4.3测定
取相同体积的试液和2-乙基蒽醌标准溶液分别注入高效液相色谱仪,根据保留时间定性,外标峰面积法定量。
2.5回收率试验
准确吸取清水板栗罐头的汤汁10ml,置于50ml容量瓶中,用蒸馏水稀释至刻度,各吸取5.0ml于5个10ml容量瓶中,分别加入浓度为0.2000mg/ml的2-乙基蒽醌对照溶液0.0ml,1.0ml,2.0ml,3.0ml,4.0ml,5.0ml,稀释至刻度,进20ul样品。利用色谱工作站计算检测结果,并人工计算回收率。结果见表2。

表2食品中2-乙基蒽醌检测的加标回收率试验结果
讨论
由于双氧水具有很强的氧化性,可以氧化食品中的一些有机物,且双氧水本身不稳定,因此,对于双氧水检测的加标回收率不尽人意。但是,此方法可判断食品中是否含有双氧水。2-乙基蒽醌检测的加标回收率是理想的。后一检测方法能方便地判断食品中是否添加了工业级双氧水。
参考文献
[1] 王增荣. 气相色谱法测定精制2-乙基蒽醌纯度[J]. 大氮肥.2003,26(4).
[2] 晁国胜.高效液相色谱法测定精制2-乙基蒽醌纯度[J].黎明化工,1993,(4).
[3] 李学梦,蔡志伟,洪洁. 双氧水生产蒽醌工作液的高效液相色谱分析方法[J].化工进展,2004 ,Vol.23 No.9 P.1019-1021.
[4] 郭升平. 高效液相色谱法测定蒽醌[J]. 精细石油化工, 1996,(1).
[5] C. Prand, T. Venrurl, J. Chromatogr. Sci.19, 308(1981).
[6] P. Jandera, J. Churacek, B. Taraba, J.Chromatogr. 262, 121(1983).
[7] R. Gloor, E. L. Jlhnson, J. Chromatogr. Sci.15, 413(1977).
[8] A. T. Hunter, J. Chromatogr. 319,319(1985).
[9] P. Janderg, J. Characek, J. Chromatogr. 197,181(1980).
(作者单位:湖北黄冈职业技术学院 湖北省黄石市产品质量监督检验所)